Science:心脏发育暗藏的"生物光缆"如何颠覆医学认知?
来源:生物探索 2025-03-19 09:49
这项研究揭示了胚胎心脏中一个令人惊叹的微观世界:心肌细胞伸出比头发丝细千倍的管状结构,穿越心胶质的汪洋,直接与心内膜细胞建立物理连接。
胚胎在形成最初的心跳时,那些精密如瑞士钟表的心脏结构究竟是如何构建?传统理论认为,心肌层与心内膜层这两大心脏组织被300微米厚的"心胶质"永久隔绝,只能依靠飘散在基质中的信号分子隔空对话。但3月14日《Science》杂志的一项突破性研究“Tunneling nanotube–like structures regulate distant cellular interactions during heart formation”,揭开了生命真正的魔术——心肌细胞竟能伸出纳米级的"生物光缆",穿透看似不可逾越的屏障,与心内膜细胞建立物理连接!
研究团队通过基因编辑小鼠模型与冷冻电镜技术,首次捕捉到胚胎心脏中神秘莫测的隧道纳米管样结构(Tunneling Nanotube-Like Microstructures,TNTLs)。这些直径不足500纳米、相当于艾滋病毒大小的管状突起,承载着Notch、VEGF等关键信号分子,以每秒0.5微米的速度在细胞间精准投递生命指令。更惊人的是,当研究人员敲除调控细胞骨架的CDC42基因,这些"纳米光缆"便会集体断裂,导致胚胎心脏丧失标志性的小梁结构,宛如被抹平指纹的光滑镜面——这正是30%先天性心脏病患者的病理特征!
这项发现不仅解开了困扰发育生物学界50年的"心脏形态发生之谜",更揭示了细胞通讯的量子跃迁:在纳米尺度上,生命竟演化出堪比光纤网络的信号高速公路。想象未来医生通过修复这些微观管道治疗先天心脏病,或利用仿生纳米管实现心肌再生,此刻实验室里的小鼠心脏成像,或许正孕育着改写人类命运的技术革命。这束穿透心胶质的纳米之光,是否将照亮再生医学的新纪元?
生命最初的乐章:心脏如何编织精密网络?
在胚胎发育的早期,心脏如同一首精妙的交响乐,每个细胞都精准地执行着命运指令。传统理论认为,心肌层(myocardium)与心内膜(endocardium)这两层心脏组织被一层名为"心胶质(cardiac jelly)"的无细胞基质物理隔开,只能通过分泌信号分子进行远距离交流。然而,《Science》发表的最新研究,彻底颠覆了这一认知——研究人员首次捕捉到连接心脏两层组织的纳米级"生物光缆",并将其命名为隧道纳米管样结构(Tunneling Nanotube-Like Microstructures, TNTLs)。
这项研究揭示了胚胎心脏中一个令人惊叹的微观世界:心肌细胞(cardiomyocytes, CMs)伸出比头发丝细千倍的管状结构,穿越心胶质的汪洋,直接与心内膜细胞(endocardial cells, ECs)建立物理连接。这些直径仅300-500纳米、长度可达10微米的"生命光缆",不仅承载着信号分子的运输,更直接决定了心脏小梁(trabeculae)的形成——那些像山脉般起伏的心室壁结构,正是人类心脏高效泵血的核心设计。
显微世界的震撼:3D成像捕捉"细胞触手"
研究团队运用遗传标记技术(genetic labeling)与成像手段,将小鼠胚胎心脏的发育过程转化为一场视觉盛宴。通过NKX2.5基因启动子驱动的荧光标记系统,研究人员在胚胎第8天(E8.0)就捕捉到心肌细胞伸出的管状突起。这些结构如同深海章鱼的触手,穿透富含透明质酸的心胶质,精准锚定在心内膜细胞表面。
更令人惊叹的是冷冻电子断层扫描(cryo-ET)呈现的纳米级细节:在三维重构图像中,TNTLs内部充满肌动蛋白(actin)纤维束,并携带运输囊泡。这种结构既不同于培养细胞中的隧道纳米管(TNTs),也不同于果蝇的细胞丝(cytonemes),而是展现出独特的生物学特征——它们不依赖基质支撑,却能跨越相当于细胞自身数倍的距离建立连接。
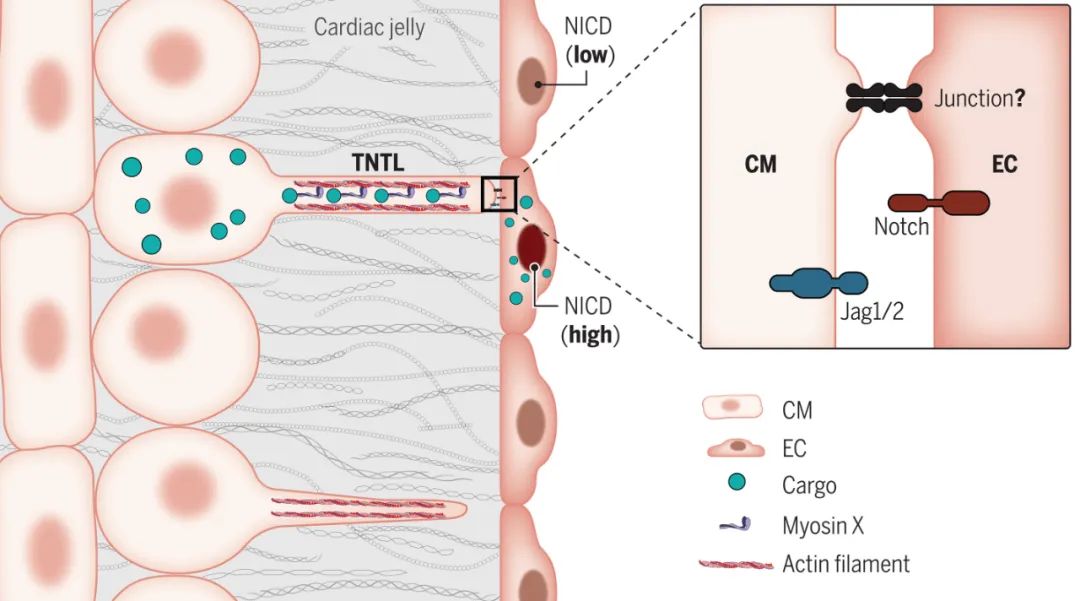
模式图(Credit: Science)
信号传递的量子跃迁:Notch通路如何被激活?
传统理论认为,Notch信号通路的激活需要细胞间直接接触。但研究数据给出了更精妙的答案:当心肌细胞通过TNTLs触碰心内膜细胞时,Notch配体(如Jag1/Jag2)像特快专递般沿管腔运输,触发心内膜细胞内的Notch1受体切割,释放出激活基因表达的N1ICD片段。实验显示,抑制TNTL形成会使Notch信号强度降低40%,而人工过表达肌动蛋白相关蛋白MyoX,则能让信号传递效率提升近3倍。
这种纳米级精准投递,解释了为何胚胎心脏能在极短时间内完成形态构建。当研究人员用药物CK-666阻断肌动蛋白聚合,胚胎心脏不仅失去小梁结构,连心室壁也变得光滑如镜——这正是多种先天性心脏病的典型特征。
基因剪刀下的心脏密码:Cdc42如何主宰形态发生?
为了验证TNTLs的功能,团队构建了心肌特异性敲除Cdc42基因的小鼠模型(MCKO)。这个编码细胞骨架调控蛋白的基因,被证明是TNTLs形成的"总工程师"。在胚胎第8.75天,正常心脏每100个心肌细胞能伸出19条TNTLs,而MCKO小鼠仅剩6条。更惊人的是,这些残缺的管状结构直径膨胀至600纳米,运输效率大幅下降。
基因层面的改变直接反映在宏观形态:MCKO小鼠胚胎的心脏小梁完全消失,心室壁薄如蝉翼。这一发现不仅印证了TNTLs的发育必需性,更揭示了约15%人类先天性心脏病可能与此通路相关——那些临床常见的"心室肌致密化不全"病例,或许正源于这些纳米管道的发育缺陷。
分子世界的快递网络:生命如何实现精准投递?
通过荧光漂白恢复技术(FRAP),研究人员首次捕捉到信号分子在TNTLs内的定向运输。当Jag1-eGFP标记的配体从心肌细胞端注入,荧光信号以每秒0.5微米的速度单向流动,整个过程如同微观世界的高速公路。更令人称奇的是,26kDa的LifeAct蛋白能通过TNTLs进入心内膜细胞,而268kDa的MyoX蛋白却始终驻留管道内部——这种分子量选择性运输,揭示了纳米管道存在精细的"海关系统"。
研究还发现,除了Notch信号,VEGF、NRG1、Angiopoietin等关键通路都依赖TNTLs进行信号放大。当这些"分子快递"同时受阻,心脏发育将陷入全面停滞——这解释了为何单一基因突变常引发多重心脏畸形。
改写教科书的启示:从胚胎学到再生医学
这项发现颠覆了发育生物学的三个传统认知:
远距离信号传递:细胞间无需直接接触,通过纳米管道即可实现膜受体-配体交互;
形态发生机制:心脏小梁并非单纯力学塑造,而是TNTLs引导的定向生长;
进化保守性:哺乳动物发展出不同于低等生物的独特细胞通讯策略。
更激动人心的是临床转化前景:通过调控TNTLs的形成,未来或能修复先天性心脏缺损,甚至增强心梗后的组织再生。研究团队已着手开发靶向CDC42的小分子激活剂,计划在大型动物模型中进行验证。
未解之谜与未来征途:生命科学的全新边疆
尽管取得突破性进展,TNTLs仍充满未解之谜:
这些纳米管道如何精准识别目标细胞?是否存在"分子邮政编码"系统?
囊泡运输的驱动力来自何种分子马达?
成年心脏是否保留TNTLs?它们在心脏修复中扮演何种角色?
生命系统的精妙远超想象。那些曾经被视作"细胞间质"的空白区域,实则充满动态的纳米级对话。研究人员掀开了细胞通讯世界的冰山一角。这些纳米级生命基建,或许将引领下一代生物技术的发展。
从心脏发育到癌症转移,从神经退行性疾病到免疫调控,TNTLs的发现为我们理解生命本质打开了全新维度。当我们凝视胚胎心脏跳动的荧光图像,看到的不仅是生命的起点,更是未来医学的璀璨星空。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


